Ciencia y Salud, Vol. IV, No. 2, mayo-agosto, 2020 • ISSN (impreso): 2613-8816 • ISSN (en línea): 2613-8824 xxx • Sitio web: https://revistas.intec.edu.do/
CORRELACIÓN ENTRE BILIRRUBINA SÉRICA TOTAL Y BILIRRUBINA TRANSCUTÁNEA EN RECIÉN NACIDOS INGRESADOS EN EL ÁREA DE NEONATOLOGÍA DEL HOSPITAL UNIVERSITARIO MATERNIDAD NUESTRA SEÑORA DE LA ALTAGRACIA, FEBRERO-ABRIL 2018, SANTO DOMINGO, REPÚBLICA DOMINICANA
Correlation between total seric bilirubin and transcutaneous bilirubin in newborn admitted in the neonatal area of the Maternidad Nuestra Señora de la Altagracia University Hospital, February-April 2018, Santo Domingo, Dominican Republic
Cómo citar: Esquea-Guerrero E, Duke-Torres W, Chevalier-Macarrulla A. Correlación entre bilirrubina sérica total y bilirrubina transcutánea En recién nacidos ingresados en el área de neonatología del Hospital Universitario Maternidad Nuestra Señora de la Altagracia, febrero-abril 2018, Santo domingo, República Dominicana. cysa [Internet]. 16 de junio de 2020 [citado 17 de junio de 2020];4(2):55-63. Disponible en: https://revistas.intec.edu.do/index.php/cisa/article/view/1763
Introducción
La ictericia, en general, es un concepto médico con el que se designa la coloración amarillenta de piel y mucosas ocasionada por el depósito excesivo de bilirrubina, la cual es un producto catabólico del metabolismo del hem, que se forma por la descomposición del grupo heme presente en la hemoglobina, la mioglobina, los citocromos, la catalasa, la peroxidasa y la triptófano pirrolasa. Por otra parte, la hiperbilirrubinemia es una noción bioquímica que indica una cantidad de bilirrubina plasmática por encima a la normalidad.1, 2,3
Se considera ictericia cuando los niveles de bilirrubina sérica sobrepasan los 12.9 mg/dl (10 mg/dl a partir de la primera semana de vida postnatal) en el recién nacido (RN) a término y 15 mg/dl en el RN pretérmino (10 mg/dl a partir de la segunda semana de vida postnatal); la concentración sérica de bilirrubina requerida para causar ictericia varía según el tono de la piel y la región corporal, pero la ictericia suele ser visible en las escleróticas cuando la bilirrubina alcanza una concentración de 2-3 mg/dL (34-51 μmol/L) y en la cara con alrededor de 4-5 mg/dL (68-86 μmol/L).4,5
Grosso modo, se puede decir que la ictericia neonatal está íntimamente relacionada con la edad gestacional, así como a patologías coexistentes, tipo de alimentación, raza y área geográfica; se calcula que el 60-70 % de los neonatos a término y 80 % o más de los pretérmino la presentarán durante los primeros 7 días de vida posnatal, convirtiéndola de esta manera, en la afección más frecuente en el recién nacido.1,3,6
En la mayoría de los casos suele ser benigna, pero existen situaciones en las que la ictericia puede ser producida por una enfermedad subyacente, como es el caso de la incompatibilidad de grupo sanguíneo o de factor Rh entre la madre y el RN. Además, la hiperbilirrubinemia indirecta en sangre traspasa la barrera hematoencefálica, siendo potencialmente nociva para el sistema nervioso central, ocasionando parálisis cerebral extrapiramidal, así como trastornos de la mirada, hipoacusia sensorioneural y displasia del esmalte dental, mientras que la hiperbilirrubinemia directa refleja graves trastornos hepáticos o sistémicos. Esto hace que tanto su reconocimiento como una instauración temprana de tratamiento sea primordial en su pronóstico.3,7-11
En el medio hospitalario de la República Dominicana, el alto índice de casos de ictericia y la corta estancia hospitalaria (4-12 horas) postnatal, exigen contar con un método rápido y seguro para la medición de la bilirrubina en el RN, aparte de los métodos estándares ya establecidos para medir la ictericia; entre ellos, la inspección visual y las pruebas de laboratorios clínicos, estas últimas, aunque son un método más objetivo, tienen algunas desventajas como la falta de relación temporal entre la extracción y el reporte de la misma, —pudiendo dificultar su interpretación—; el alto costo que representan para el hospital o el paciente; y que la toma rutinaria de sangre se asocia a un mayor riesgo de infección además de que significa un proceso doloroso para el RN. Es por ello, que los lectores de bilirrubina transcutánea son una opción deseable, tanto por su facilidad de uso como por la posibilidad de tener una lectura inmediata con resultados rápidos para la toma de decisiones terapéuticas en la mayor brevedad posible, disminuyendo los procesos invasivos en el paciente. Adicionalmente, estos han demostrado ser muy útiles como instrumentos de monitoreo, motivo por el cual durante las últimas dos décadas se ha extendido su uso a nivel internacional. No obstante, diversos estudios difundidos han demostrado que su exactitud podría variar según las características físicas, edad gestacional y días de vida postnatal del RN.12,13
A causa de esto, se hace importante realizar estudios nacionales, adecuados a las características de la población, determinando así la utilidad y precisión de la bilirrubina transcutánea en los RN del país.
Material y Métodos
Tipo de estudio
Se llevó a cabo un estudio observacional, descriptivo y transversal de recolección prospectiva de datos, con el propósito de determinar la correlación entre la bilirrubina sérica total y la bilirrubina transcutánea, en recién nacidos ingresados en el área de neonatología del Hospital Universitario Maternidad Nuestra Señora de la Altagracia, durante el periodo febrero-abril 2018.
Población y muestra
La población estuvo formada por todos los neonatos ingresados en el área de neonatología del Hospital Universitario Maternidad Nuestra Señora de la Altagracia durante el periodo del estudio, y la muestra estuvo constituida por los neonatos ictéricos y/o con solicitud de examen de bilirrubinas séricas, ingresados en el área y que cumplían con los criterios de inclusión.
Criterios
1. De inclusión
Se incluyó en este estudio a todo recién nacido ictérico y/o con solicitud de bilirrubinas séricas, con edad gestacional igual o mayor a 28 semanas, con edad postnatal entre 1 y 30 días de vida, que no haya recibido fototerapia al momento de las mediciones y al cual el investigador pudo tomar la bilirrubina transcutánea simultáneamente a la sérica, con un margen no mayor a 30 minutos.
2. De exclusión
Se excluyó a todo recién nacido que no contara con solicitud de bilirrubina sérica o que no estuviera ingresado en el área de neonatología.
De igual manera, se descartaron aquellos neonatos que recibieron exanguinotransfusión, fototerapia, albúmina o fenobarbital al momento de las mediciones.
Instrumento de recolección de los datos
Se diseñó un instrumento de recolección de datos con un total de once preguntas directas sobre las informaciones personales del recién nacido: número de identificación, sexo, nacionalidad, color de piel, edad gestacional, días de vida postnatal, peso, talla, valor medido por el bilirrubinómetro transcutáneo y valor medido por el laboratorio clínico de la bilirrubina sérica total.
Procedimientos
Una vez identificados los pacientes, la muestra sanguínea fue obtenida por el residente de neonatología encargado del área, mientras que las muestras transcutáneas fueron tomadas con el bilirrubinómetro Kejian KJ-8000. Los datos personales del paciente fueron recolectados por la encargada de esta investigación. Previo al inicio de recolección de datos se solicitó la autorización al Departamento de enseñanza y perinatología del hospital, por escrito.
Tabulación y análisis
Las operaciones de tabulación se realizaron, en primer lugar, de forma manual y, posteriormente, fueron tabuladas a través Microsoft Word y Excel para el diseño y manejo de datos. Dichos resultados fueron presentados en gráficas y tablas de porcentajes para mayor compresión. Los datos se analizaron utilizando la medida de tendencia central y para la correlación entre las determinaciones de bilirrubina trascutánea y la sérica se utilizó la R de Pearson, en la cual la correlación positiva se demuestra mientras r se acerca más a 1.
Aspectos éticos
Este estudio fue realizado bajo las normativas éticas internacionales, tomando en cuenta los principios establecidos en la declaración de Helsinki y las pautas del Consejo de Organizaciones Internacionales de las Ciencias Médicas (CIOMS). Toda información incluida en el presente texto, tomada de otros autores, fue justificada por su llamada correspondiente.14, 15
Resultados
Gráfica 1. Distribución de los pacientes sometidos al estudio de la medición de bilirrubina transcutánea y sérica. Según el sexo

Discusión
Durante el el periodo de estudio, se evaluaron un total de 30 pacientes ingresados en el área de neonatología de Hospital Universitario Maternidad Nuestra Señora de la Altagracia, que cumplieron con todos los criterios de inclusión. A los mismos se le realizó la toma de bilirrubina transcutánea frontal y central (esternón) con no más de 30 minutos de diferencia a la recolección de muestra sanguínea para realizar la prueba de bilirrubinas séricas.
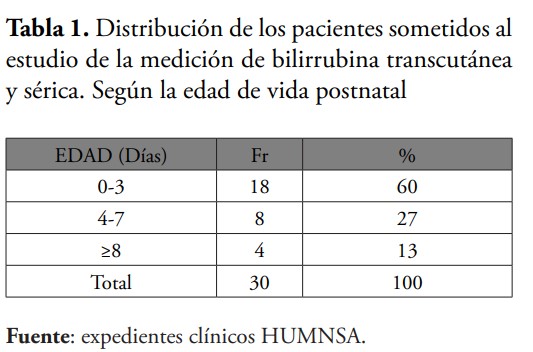
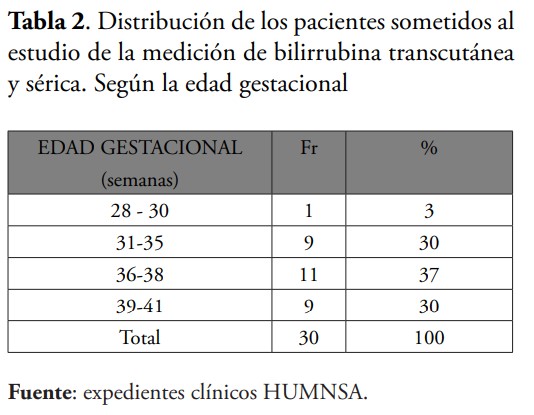
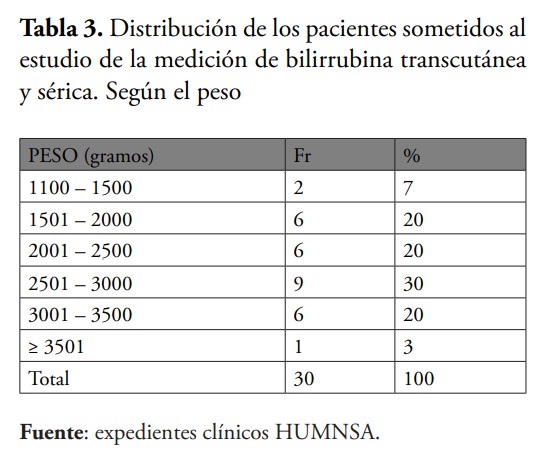
Al recolectar la muestra para el estudio, se observó que el sexo más frecuente fue el masculino, representando un 63.3 % de los pacientes, así como que el 60 % de los neonatos tenían menos de 3 días de vida postnatal al momento de presentar la hiperbilirrubinemia. De igual manera, se identificó que el rango de edad gestacional más frecuente fue de 36-38 semanas y que el promedio de peso de los recién nacidos evaluados fue de 2,478 g. Esto concuerda con una investigación realizada por Bernal en el año 2013 en México, donde se evaluaron un total de 33 pacientes, de los cuales 60 % fueron masculinos, 50 % tenía menos de 2 días de vida postnatal y el peso promedio fue de 2,977 g.1 Estos resultados también coinciden con la lectura internacional en cuanto el perfil epidemiológico de los recién nacidos que desarrollan ictericia.
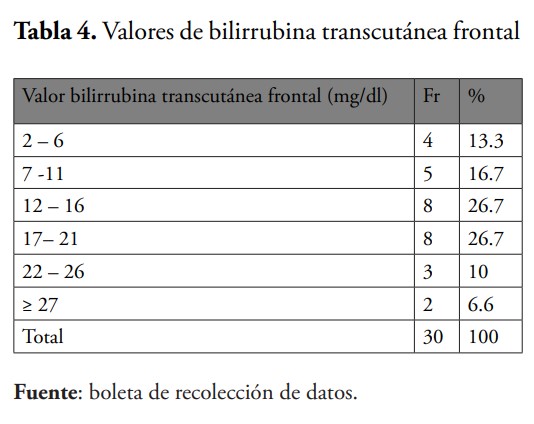
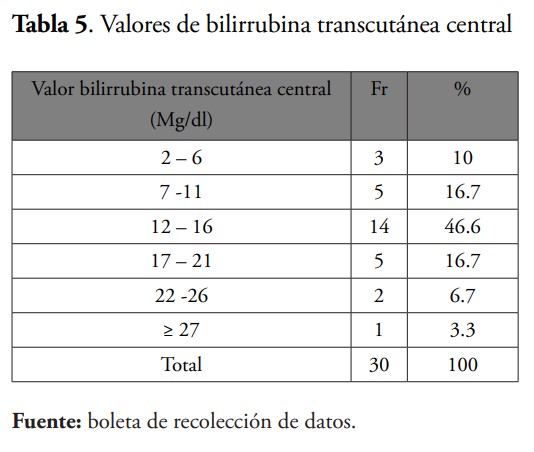
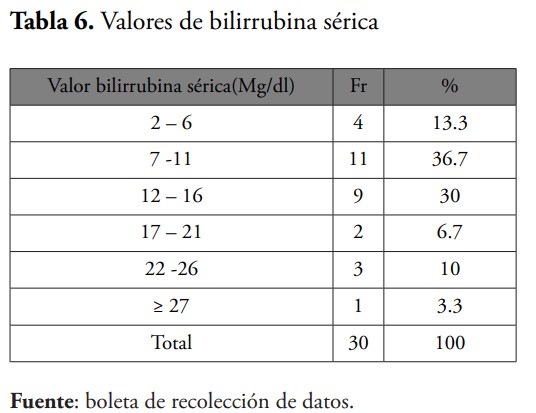
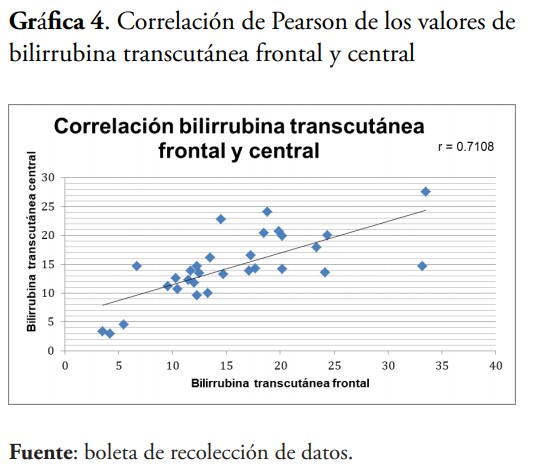
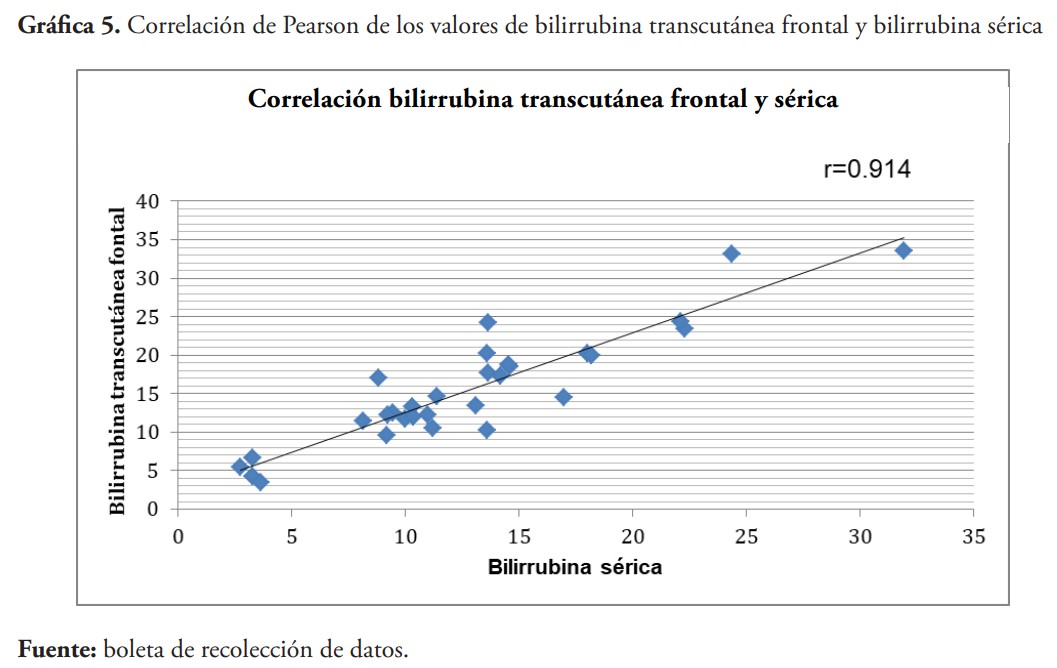
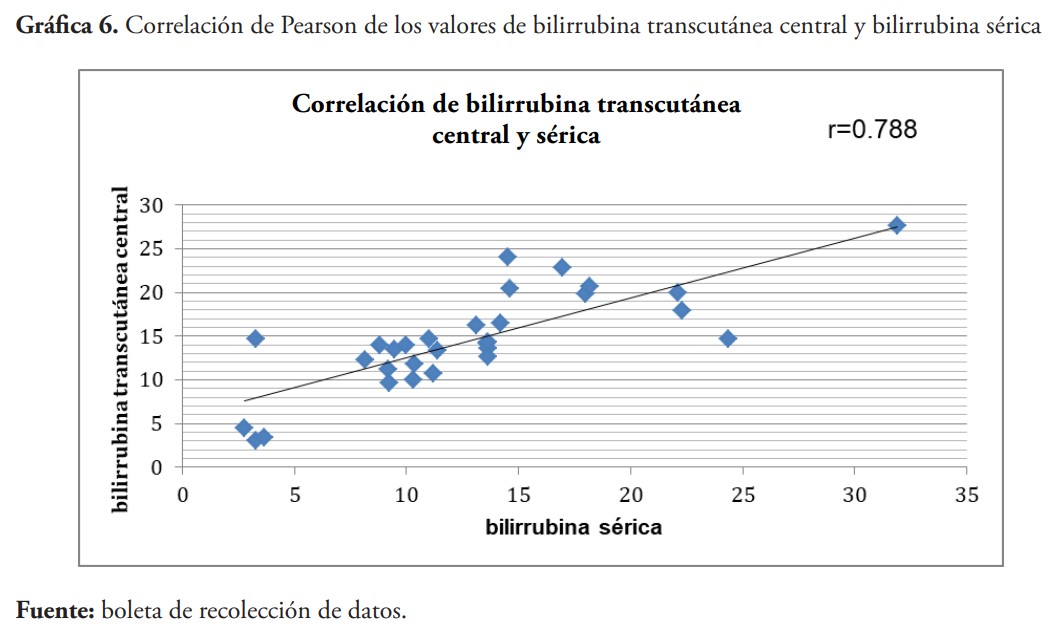
En esta investigación la media de bilirrubina transcutánea frontal (Bttf) fue 15.56 mg/dl, en bilirrubina transcutánea central (Bttc) fue de 14.53 mg/dl, mientras que en la bilirrubina sérica fue de 12.89 mg/dl. Al momento de evaluar la correlación entre las mediciones observamos que las Bttf y Bttc obtuvieron una concordancia de Pearson de 0.71, la Bttf y la sérica fue de 0.91, siendo la mayor concordancia, mientras que en la Bttc y la bilirrubina en sangre fue de r=0.78. Por lo que se encontró que a pesar de que los niveles resultados de la medición transcutánea no son exactos, están muy cercanos a aquellos derivados de la medición de bilirrubinas séricas. Además, los valores de concordancia de este estudio coinciden con una investigación publicada por Martínez Mercado et al., en el año 2014 en México, en la cual se obtuvo una correlación de Bttf/sérica de 0.8411 y de Bttc/sérica de 0.7942.16
Por otro lado, la literatura internacional plantea que los valores otorgados por la bilirrubinometria transcutánea suelen discrepar de los resultados de la bilirrubina sérica entre 2–3 mg/dl.1 Al comparar los resultados de las 3 muestras tomadas en esta investigación se percibió que la diferencia ente Bttf y la sérica, en promedio, era de 2.67 mg/dl, mientras que la Bttc y la sérica tenían una media de disconformidad de 1.64 mg/dl.
Esta diferencia menor que se observa entre la muestra tomada en esternón y la bilirrubina en sangre, posiblemente sea debida a que la ropa del niño protege su pecho de los rayos ultravioleta del sol que entran por las ventanas del área de internamiento conjunto, las cuales destruyen las moléculas de bilirrubina que se encuentran en la piel, provocando una lectura transcutánea alterada de los lugares que no estén protegidos de los rayos solares, regularmente, dando valores elevados en relación con la sérica.10 Bernal, en el año 2013 en México, obtuvo en su estudio resultados parecidos a esta investigación, en su caso la medición frontal varió 1.5 mg/dl respecto a la sérica, y la medición central alrededor de 1.2 mg/dl.1
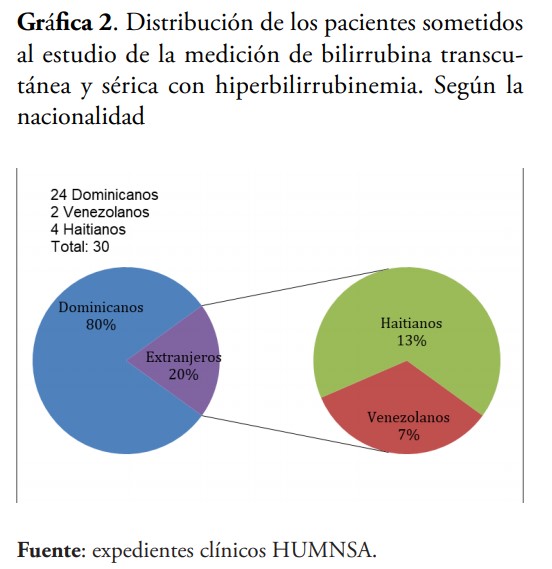
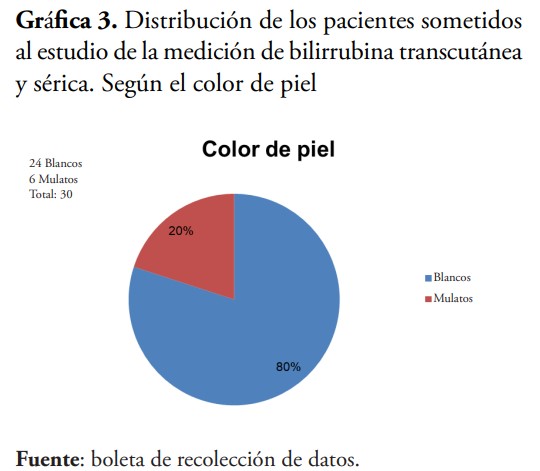
Durante la investigación también se observó que los pacientes de piel blanca tenían en general menor discrepancia entre las muestras (1.595 mg/dl) que los neonatos de piel mulata (4.443 mg/dl); esto se debe a que los valores dados por la lectura de bilirrubina transcutánea están influenciados por la pigmentación de la piel, ya que el espectro de luz devuelto, dependerá de varios cromóforos cutáneos, como son la melanina, el colágeno, la hemoglobina y, por supuesto, las bilirrubinas; por esto, a mayor melanina, menor capacidad de que las ondas enviadas por el aparato registre la pigmentación amarrilla en la piel.12
Al evaluar detenidamente la discrepancia entre los valores, se encontró que en aquellos pacientes con edad gestacional entre las 35 y 38 semanas existía una diferencia de Bttf/sérica y Bttc/sérica menor que los recién nacidos con mayor o menor edad gestacional, en este grupo el promedio de discordancia fue de 2.27 mg/dl y 2.12 mg/dl, respectivamente; además se observó que en aquellos neonatos que tenían menos de 3 días de vida posnatal, la similitud entre los valores de las pruebas era mayor.
En resumen, los resultados conseguidos en esta investigación son semejantes a los publicados en otros estudios en los que se ha utilizado como screening y estos datos son plausibles para la práctica diaria.
Conclusión
Luego de analizar y discutir los resultados de esta investigación, se encontró que los niveles provenientes de las muestras transcutáneas no son exactos, pero son lo suficientemente cercanos a los resultados de las bilirrubinas séricas. De igual manera se comprobó que el tomar ambas muestras transcutáneas permite alcanzar una predicción más certera de bilirrubinas séricas.
Por lo tanto, los bilirrubinómetros transcutáneos pueden ser utilizados como una herramienta del monitoreo de bilirrubina en neonatos con riesgo de hiperbilirrubinemia e ictericia; reduciendo el número de procesos invasivos, estancia hospitalaria y, a su vez, permitir la toma de decisión de iniciar el tratamiento con fototerapia o dar el alta.
Referencias
- Bernal Tovar C. (2013). Estandarización de bilirrubinómetro transcutáneo comparado con bilirrubinas séricas en recién nacidos del Hospital General Ecatepec Las Américas Isem [tesis de posgrado-Pediatría]. Hospital General de Ecatepec Las Américas, Toluca, Estado de México: Disponible en: http://ri.uaemex.mx/handle/20.500.11799/14219
- Progeny. Managing Newborn Hyperbilirubinemia and Preventing Kernicterus. 2013;29(1). Disponible en: http://publications.iowa.gov/14704/1/progeny_june2013.pdf
- Campos A, Alonso RM, Amador R, Ballesté I. Comparación de dos métodos diagnósticos de ictericia neonatal. Rev Cubana Pediatr. 2012;84(1):70-1. Disponible en: http://scielo.sld.cu/scielo.php?pid=S003475312012000100007&script=sci_arttext&tlng=pt
- OPS/PMS. Guía para el manejo integral del recién nacido grave. Guatemala; 2015. Disponible en: http://www.paho.org/gut/index.php?option=com_docman&view=document&slug=guia-para-el-manejo-integral-del-recien-nacido-grave&%20layout=default&alias=773-guia-para-el-manejo-integral-del-recien-nacido-grave&category_%20slug=boletines-en-web&Itemid=518
- Ruiz J, Pérez M, Toledo B, Zozaya C, Remesal A. Manual CTO de medicina y cirugía. Pediatría. (9a ed.). Madrid: CTO editorial, S.L.; 2014.
- Colombiana de Salud S.A. Guía de atención manejo de ictericia neonatal. Revisión 01. 2014;2. Disponible en: http://www.colombianadesalud.org.co/GUIAS_MEDICINA_ESPECIALIZADA/PEDIATRIA/GUIA%20ICTERICIA%20%20NEONATAL%202014.pdf
- Jospe N. Hiperbilirrubinemia neonatal. En: Manual Merck. Estados Unidos; 2015. Disponible en: https://www.google.com.do/search?q=ictericia+fisiologica&lr=&dcr=0&tbs=cdr:1,cd_min:2013&ei=D90NWqjmKZfUjwPb5KCQCQ&start=10&sa=N&biw=1607&bih=766
- Faz Garza JC. (2014). Correlación de bilirrubinas séricas y transcutáneas en recién nacidos sanos del alojamiento conjunto del Hospital General de Tlalnepantla Valle Ceylan, de noviembre del 2012 a octubre del 2013 [tesis de posgrado-Pediatría]. Hospital General de Tlalnepantla Valle Ceylan, Toluca, Estado de México. Disponible en: http://ri.uaemex.mx/bitstream/handle/20.500.11799/14915/Tesis.418127.pdf?sequence=1
- Grosse C, Simeoni U. Hperbilirrubinemia en el recién nacido Prematuro. EMC – Pediatría. 2012;47(4):1-3. Disponible en: http://www.sciencedirect.com/science/article/pii/S1245178912635215
- Hernández M, Schmidt I, Huete l. Encefalopatía por Kernicterus. Serie clínica Kernicterus (bilirubin encephalopathy): case reports. Rev. chil. Pediatr. 2013;84(6). Disponible en: http://www.scielo.cl/scielo.php?pid=S037041062013000600009&script=sci_arttext
- Rivera L, Esquea E, Rosa Arias A, Mireya Jiménez L, et al. Normas de las principales urgencias peri-neonatales [Series de normas nacionales No. 27]. Santo Domingo, República Dominicana: Secretaría de Estado de Salud Pública y Asistencia Social; 2003. Disponible en: http://www.msp.gob.do/oai/documentos/Normas%20y%20Reglamentos/Normas/MATERNO%20%20INFANTIL/URGENCIAS-PERI-NEONATALES.pdf
- Méndez Soveranis S. (2015). Correlación entre la medición de bilirrubina transcutánea y la medición de bilirrubina sérica en recién nacidos con ictericia (tesis de posgrado-Pediatría). Universidad de San Carlos de Guatemala, Guatemala. Disponible en: http://biblioteca.usac.edu.gt/tesis/05/05_9542.pdf
- García H, Torres-Gutiérrez J, Peregrino-Bejarano L, Cruz-Castañeda MA. Factores de riesgo asociados a infección nosocomial (IN) en una Unidad de Cuidados Intensivos Neonatales (UCIN) de tercer nivel. Gac Med Mex. 2015;151:711-9. Disponible en: http://www.anmm.org.mx/GMM/2015/n6/GMM_151_2015_6_711-719.pdf
- Manzini JL. Declaración de Helsinki: principios éticos para la investigación médica sobre sujetos humanos. Acta bioethica. 2000;IV(2):321.
- International ethical guidelines for biomedical research involving subjects. Prepare by the council for international organization medical sciencies (CIOMS) in collaboration with the World Health Organization (WHO) Genova; 2002.
- Martínez-Mercado M, Torres-Bernal LF, Góngora-Ortega J, Sánchez-Ortiz M, Guerrero-Díaz de León JA. Medición simultánea de bilirrubina total transcutánea en frente y esternón como modelo predictivo de bilirrubina total sérica en recién nacidos prematuros y de término. Acta Pediátr Mex. 2014;35:118-24. Disponible en: https://www.medigraphic.com/pdfs/actpedmex/apm-2014/apm142e.pdf

