Introducción
El estudio de la presencia de metales pesados en aguas de ríos y sedimentos, constituye un aporte a la disposición de información de carácter ambiental de dichos ríos y contribuirá al diagnóstico de cada una de sus cuencas y por consiguiente a facilitar la toma de decisiones sobre todo de carácter gubernamental . Los metales pesados constituyen un serio problema ambiental debido a su toxicidad y a sus repercusiones fisiológicas tanto en los seres humanos como en animales, tal es el caso de los peces. La investigación de la presencia de metales pesados en determinadas aguas, permite conocer las rutas de contaminantes y su interacción con otras sustancias presentes en las aguas.
Durante el período comprendido entre el 6 de Octubre del 2002 y el 7 de Septiembre del 2003, se ejecuto el proyecto sobre determinación de metales pesados en aguas y sedimentos del río Haina. El proyecto fue financiado por el departamento de investigaciones y publicaciones del Intec y fue ejecutado por un equipo técnico formado por los profesores Dr. José Contreras, Lic. Leticia Mendoza y Lic. Arismendis Gómez como analista.
Justificación
Debido a su toxicidad la presencia de metales pesados en aguas y sedimentos de ríos representa un serio problema de salud para los moradores de las poblaciones que se sirven de dichos ríos, lo cual implica elevar los gastos en tratamientos médicos, disminución de l a capacidad productiva de los moradores y desde luego repercusiones económicas a nivel local y nacional. La contaminación por Plomo y por Cadmio afecta al sistema nervioso central, lo cual se traduce en retraso mental. Esto tiene particular importancia sobre todo en la población infantil y adolescente pues está asociado al desarrollo de la capacidad intelectual de la población afectada y a la larga tendría un serio impacto en el intelecto de los dominicanos y por consiguiente en las posibilidades de desarrollo a todos l os niveles de la República Dominicana. El conocimiento pues de los niveles de contaminación por metales pesados permitiría la toma de decisiones adecuadas en el campo de l a salud, el medio ambiente y en general en el plano social repercutiendo positivamente en la realidad nacional dominicana.
El Río Haina es uno de los ríos más importantes de la República Dominicana y recibe efluentes domésticos e industriales de los barrios y zonas industriales ubicados al oeste de la ciudad de Santo Domingo. Este río desemboca en el Mar Caribe, por lo que contribuye a la contaminación de la costa sur dominicana, sobre todo el área costera comprendida entre el Distrito Nacional, la Provincia Santo Domingo y la Provincia San Cristóbal.
Antecedentes bibliográficos
Obiols, Devesa, Peiro y Salayet( 13) desarrollaron el concepto de especiación de metales pesados por medio del cual se analiza la presencia de ellos bajo diferentes formas químicas en agua dulce y agua de mar. El concepto de especiación implicaba el análisis de dichos metales en forma lábil o suelta, en disolución, formando complejos, asociado a partículas, asociado a materia orgánica o inorgánica o como metal total. En un trabajo posterior, los mismos autores(14) aplicaron la metodología desarrollada a los análisis de cobre, plomo y cadmio en muestras de agua de mar de l a zona frente a la ciudad. de Barcelona, España.
Romana Ruíz (15) abordó el problema de la contaminación de sedimentos marinos en función de la discusión de los efectos ambientales de las operaciones de dragado en las obras portuarias y marinas.
La disminución de la población de salmones en las aguas del río Bidasoa en España fue atribuida por Ruiz, Romero y Echeandía( 16) a la composición del sedimento de dicho río, en el cual fueron encontrados elevados niveles de cadmio, cobre, zinc y cromo.
La adsorción de metales pesados en resinas de intercambio catiónico fue estudiada por El Kady, Ahmadi y Odozi(8) estudiándose los efectos de la concentracióniónica y del pH en dicho comportamiento de adsorción. Por su parte Campos y Néstor(5) estudiaron los niveles de metales pesados en el pez Ariopsisbonillai de la Ciénaga Grande de Santa Marta, Colombia, comprobándose en el hígado valores superiores de Zn y Cu a los determinados en el músculo. La resistencia a metales pesados tóxicos fue encontrada en bacterias de origen clín ico y ambiental por Cervantes, Chávez y Vaca(6); una experiencia similar reportaron Mondaca, Abarzua, Paredes y Maugeri ( 12).
Los procesos de movilización/deposición de metales pesados aplicados al manganeso en el sistema río Eume-embalse de La Coruña, España fueron estudiados por Bello, Souto, Casares y Domínguez (2). Dey y Dwivedi (7) encontraron elevados niveles de metales pesados en huevos de gallina en La India. La participación de metales pesados en un lago eutroficado fue objeto de estudio de Borg, y colaboradores (3) en tanto que Lazara, Moliner, Duelves y Nerin (9) exploraron las posibilidades de obtener productos valiosos a partir de residuos minerales de aceites que contienen metales pesados. La remoción del Cromo trivalente fue estudiada por Barber y Stuckey (1 ). De igual manera Brian (4) i nvestigó la remoción de diferentes metales pesados del agua y analizó su importancia ambiental.
Que la presencia de metales pesados en la sangre de determinados individuos pueden ser causa de violencia en las escuelas, es un planteamiento sostenido por Mag (10) como resultado de estudios realizados en universidades norteamericanas.
Mendoza de Cid y Naut (1 1) determinaron los niveles de diferentes elementos químicos, entre ellos metales pesados en el río Ozama de la ciudad de Santo Domingo utilizando la técnica de Fluorescencia de Rayos X por reflexión total (TR XRF), encontrando elevadas concentraciones por encima de los estándares.
Metodología
Se realizaron 8 muestreos (un promedio de 1 cada mes y medio) , abarcando una extensión de aproximadamente 12 Km. de la cuenca baja del río.
Las muestras fueron envasadas en recipientes plásticos y analizadas posteriormente por espectrometría de absorción atómica en un equipo Shimadzu 680U. Los puntos elegidos para la toma de muestras fueron los siguientes:
PUNTO 1: Batey Bienvenido (carretera ManoguayaboLa Pared) debajo del puente donde hay un balneario.
PUNTO 2: Carretera Manoguayabo Quita Sueño frente a la planta de tratamiento de la CAASD.
PUNTO 3: En Bayona (próximo a la urbanización de Bisonó).
PUNTO 4: Detrás de Engombe.
PUNTO 5: Punto Intermedio entre Guajimia y Engombe
PUNTO 6: Donde desemboca la cañada de Guajimia.
PUNTO 7: Debajo del puente de la Autopista 30 de Mayo.
PUNTO 8: Próximo al puerto de Haina (frente al club Náutico)
PUNTO 9: Punto más lejano (río arriba) al que se llega por vía acuática.
Las muestras del 1-3 se toman por vía terrestre y las restan tes por vía acuática. Las condiciones de los muestreos fueron las siguientes:
Primer muestreo: lluvias abundantes en los días anteriores y el día del muestreo.
Segundo muestreo: menos lluvias con respecto al primer muestreo. Las aguas presentan un color marrón entre los puntos 5-8. Entre los puntos 4-5 las aguas tienen un color verde intenso. Entre los puntos 4-9 el color del agua es normal.
Tercer muestreo: período de sequía. Las aguas presentan color marrón en todos los puntos.
Cuarto muestreo: periodo de sequía, en comparación con los muestreos anteriores.
El color marrón de los muestreos anteriores es mucho menos notorio.Prácticamente ha desaparecido.
Quinto muestreo: período de sequía. El río tiene poco caudal y muchas lilas en algunos tramos. El punto 3 completamente cubierto de lilas y limo.
Sexto muestreo: periodo de sequía. El río tiene muchas lilas en algunos tramos. Los puntos 1, 2 y 8 las aguas lucen bastante limpias con relación a los muestreos anteriores. El punto 3 completamente cubierto de limo.
Séptimo muestreo: período de lluvias abundantes. El río luce completamente limpio de lilas y limo y tiene mucho caudal.
Octavo muestreo :periodo de lluvias abundantes. El río luce completamente limpio de lilas y limo y tiene mucho caudal. En días anteriores al muestreo se salió de su cauce normal debido a lluvias abundantes.
Se tomaron muestras tanto en aguas superficiales del río escogido, como en sus sedimentos, las cuales fueron tratadas y conservadas en medio ácido y a determinadas temperaturas. El análisis tuvo lugar mediante la técnica de Espectrofotometría de Absorción Atómica en un equipo Marca Shimadzu Modelo 680U. Se comparan los resultados con los estándares nacionales e internacionales y se evalúan tendencia se impactos ambientales en los ecosistemas estudiados.
Resultados
Los resultados obtenidos pueden ser visualizados en las tablas 1-10 y Figs. 1-10.
Para fines de análisis tomaremos cada uno de los metales por separado dentro de un muestreo y estudiaremos el comportamiento de los niveles de concentración según punto muestra. En segundo término analizaremos para ese mismo metal los niveles de concentración en cada muestreo en un mismo punto muestra. En tercer lugar para un mismo punto muestra! y dentro de un mismo muestreo evaluaremos los niveles de concentración de cada uno de los metales investigados. Esta evaluación se hará tanto en las muestras de agua como en las muestras de sedimentos.
Metales pesados en sedimentos
Cobre
Los niveles de Cobre en el primer muestreo fueron 115.67ppm en la estación de muestreo #1; 131 .40ppm en la #2; 57.61ppm en la #3; 110.55 ppm en la #4; 64.58 ppm en la #5; 64.06 ppm en la #6; 90.37 ppm en la #7; 70.24 ppm en la #8 y 94.43ppm en la #9. Las estaciones escogidas van en orden ascendente de Norte a Sur en dirección a la desembocadura del Río Haina en el Mar Caribe. Los valores más altos fueron encontrados en las estaciones #1 , #2, #4; #7 y #9 en tanto que los valores más bajos estuvieron en las estaciones #3, 5, 6 y 8. En este primer muestreo no puede apreciarse ninguna tendencia definida en los niveles de concentración con respecto a los puntos muestrales, aunque en las estaciones ubicadas en las proximidades de la desembocadura todas las concentraciones están por debajo de 100 ppm en contraste con los valores registrados en las estaciones alejadas de la desembocadura. Esto último sin embargo no nos lleva a concluir en establecer una tendencia pues dentro de estos últimos valores se producen oscilaciones. El valor promedio de este muestreo estuvo ubicado en 88.77ppm.
En el segundo muestreo se observó un comportamiento también oscilatorio de estación a estación y el valor promedio de las estaciones fue de 76.44 ppm. En el tercer muestreo el promedio de las estaciones fue de 74.81; en el cuarto muestreo este promedio fue de 132.32 ppm; en el quinto muestreo 66.18 ppm; en el sexto 87.20 ppm; en el séptimo 73.62 ppm y en el octavo 59.58 ppm. En la mayoría de los muestreos los valores más altos fueron registrados en las estaciones #1 y #2.
Al analizar las estaciones a lo largo de los ocho muestreos realizados durante el período de tiempo investigado , los resultados encontrados son los siguientes: Para l a estación #1 el valor promedio fue 140.71 ppm; 1 13.60 para la #2 ; 64.25 ppm para la #3; 82.60ppm para la #4; 86.37 para la #5; 71 .14 pprn para l a #6; 66.28 para la #7; 57.27pprn para #8 y 59.06 para la #9. Esto muestra una tendencia descendente en las estaciones al aproximarse a la desembocadura del río.
En cuatro de las nueve estaciones se observó que en el mes de febrero se presentaban los más altos niveles de Cobre.
TABLA No. 1
Resultados presencia de metales pesados en el Río Haina Cobre en sedimentos

COBRE EN SEDIMENTOS
Plomo
En el primer muestreo los valores encontrados en las 9 estaciones fueron respectivamente 195.01ppm; l 7 l .88ppm; 785.96 ppm; 239.71 ppm; 179.62 ppm; 320.34 ppm; 166.40 ppm; 112.56 ppm y 289.79 ppm, para un promedio de las estaciones de 273.47 ppm. Se observaron valores extraordina riamente altos en las estaciones 3, 6 y 9. En el segundo mues treo realizado en Noviembre del 2002 los valores registrados fueron 197.26ppm; 76.41ppm; 181.07ppm; 12.55 ppm, 4.96 ppm; 30.04 ppm; 6.67ppm; 34.94 ppm ; 29.31 ppm y el valor promedio de las estaciones fue de 63.69 ppm. Es importante destacar que en este muestreo los valores registrados a partir de la estación #4 son considerablemente bajos, con relación a los registrados en las otras estaciones y a los de todas las estaciones en el primer muestreo. En los siguientes muestreos se observa una considerable tendencia descendente, registrándose los valores más bajos en los muestreos de Marzo y Julio del 2003. En este último mes se registraron valores por debajo del punto de detección del equipo que es 0.001 ppm.
Al analizar los datos de una misma estación a lo largo de periodo estudiado, se observan valores considerablemente altos en los primeros dos muestreos, sobre todo en las estaciones 1, 2 y 3. Se produce una tendencia descendente en los meses subsiguientes, registrándose los valores menores en Marzo y Julio 2003. Los valores promedio por estación a lo largo del período investigado fueron los siguientes 67.17 ppm para la estación #1; 49.33 ppm para la estación #2; 128.31 ppm para la estación #3; 33.04 ppm para la estación #4; 31.07 ppm para la estación #5; 67.68 ppm para la estación #6; 27 . 1 1 ppm para la estación #7; 21.44 ppm para la estación #8;y 40.93 ppm para la estación #9. Los valores promedio más altos a lo largo del año fueron para las estaciones 1, 3, 6 y 9.
TABLA No. 2
Plomo en sedimentos

PLOMO EN SEDIMENTOS
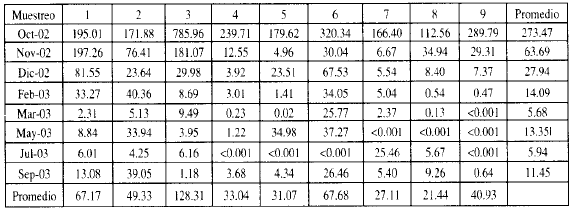
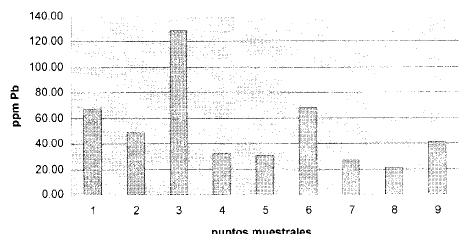
Fig. 2 Concenlraciones Promedio Pb Vs. Puntos Mueslrales
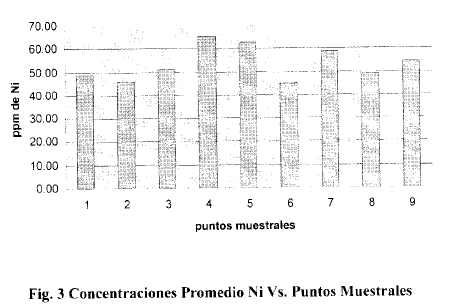
Niquel
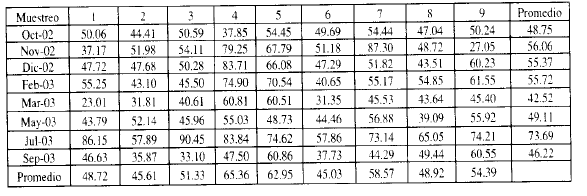
En el primer muestreo los valores de Níquel en las diferentes estaciones oscilaron entre 37.85 ppm y 54.45 ppm. El valor mínimo correspondió a la estación #4 en tanto que el valor máximo correspondió a la estación #7. El promedio para todas las estaciones fue de 48.75 ppm. En el segundo muestreo correspondiente al mes de Noviembre del 2002, se observó un incremento de los niveles de Níquel en 7 de las 9 estaciones, es decir en un 77.8 %. Sólo las estaciones 1 y 9 registraron valores inferiores al muestreo anterior. El valor promedio de las estaciones fue de 56.06 ppm. En el tercer muestreo el valor promedio fue de 55.37ppm, en el cuarto de 55.72 ppm, en el quinto 42.52 ppm, en el sexto muestreo, el promedio fue de 49.11 ppm, en tanto que en el séptimo muestreo este valor fue de 73.69 ppm, el mas alto de todos los valores obtenidos y finalmente en octavo muestreo, el valor promedio de las estaciones fue de 46.22 ppm.
Al evaluar una misma estación a lo largo del período estudiado, se observa por ejemplo en la estación #1 un valor de 50.06 ppm de Níquel en el primer muestreo, 37.17 ppm en el segundo; 47.72 ppm en el tercero, 55.25 ppm en el cuarto; 23.01 ppm en el quinto: 43.79 ppm en el sexto; 86.15 ppm en el séptimo y 46.63 ppm en el octavo. El valor promedio durante el período estudiado fue de 48.72 ppm . Es notorio que los valores menores se obtuvieron en los meses de Marzo y Septiembre del 2003 es decir en el quinto y octavo muestreo, lo cual también se refleja en los valores promedio de las esta ciones a lo largo del citado período de estudio.
TABLA No. 3
Níquel en sedimentos
NIQUEL EN SEDIMENTO
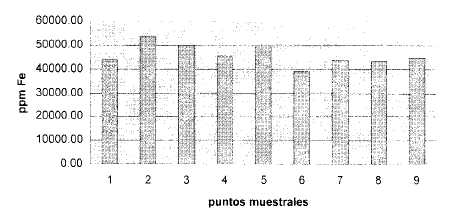
Hierro
Este metal es de todos los investigados el que mayores niveles de concentración presentó en todas las estaciones y en todos los muestreos. Sin embargo es necesario destacar que es el menos tóxico de todos.
En el primer muestreo los valores oscilaron entre 28,534 ppm y 531 16 ppm para un valor promedio de las estaciones de 41101 ppm. Los valores más altos correspondieron a las estaciones 1, 2, 3, 5 y 8. Al igual que en los otros metales no existe un patrón definido de comportamiento al comparar los resultados de una misma estación a lo largo del período investigado. A partir del valor promedio obtenido para todas las estaciones en el primer muestreo de Octubre 2002 (41191ppm), se observa un ligero descenso en Noviembre 2002 (33008.22ppm), incrementándose en Diciembre de ese año (53441.67ppm). El comportamiento de Febrero (48661.89 ppm) fue similar al de Diciembre, observándose en Marzo (38906.22 ppm) y Mayo del 2003 (38615 ppm) otro descenso, para incrementarse en Julio (53440 ppm) y Septiembre del 2003 (60641.67 ppm). En términos de las estaciones del año, parecería que en los meses de Otoño y Primavera los niveles son menores que en los meses de Verano e Invierno. Los valores promedio más altos registrados correspondieron a los meses de Septiembre, Julio y Diciembre.
TABLA No. 4
Hierro en sedimentos
HIERRO EN SEDIMENTOS

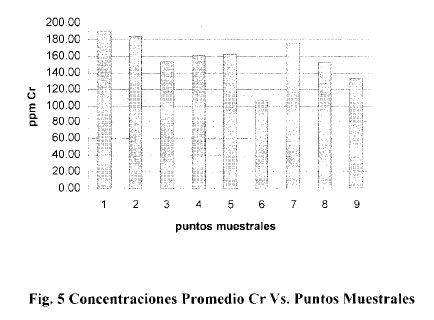
Cromo
En el primer muestreo los valores de Cromo oscilaron entre 104.46 ppm y 337.26 ppm. Los valores más altos se presentaron en l as estaciones 1, 2, 7 y 8, para un valor promedio de las estaciones de 174.76. Este promedio desciende en el mes de Noviembre (121 .36 ppm), incrementándose en el mes de Diciembre a 181.25 ppm. En febrero se mantiene próximo al valor anterior (147.58 ppm), desciende en Marzo (131.75 ppm), retomando en Mayo (143.01 ppm) a niveles próximos a los de Febrero. En Julio se produce un incremento que eleva el valor a 184.46 ppm muy similar a Diciembre. El valor registrado en Septiembre (175.15) es apenas un ligero descenso con respecto al de Julio.
Con el Cromo se produce una tendencia similar a lo ocurrido con el Hierro, es decir los máximos valores se presentan en Diciembre, Julio y Septiembre, aunque en este caso el valor promedio de Octubre es similar al de Septiembre.
El promedio anual por estación fue de 190.09 ppm para la estación #1, 184.13 ppm para la estación #2; 152.92 para la estación #3; 160.62 ppm para la #4 y 162.27 ppm para .la estación #5. En el caso de la estación #6 este valor fue de 105.57 ppm y para la estación #7 de 175.59 ppm. La estación estación #8 tuvo un promedio de 152.08 ppm, mientras que la estación #9 lo tuvo de 133.47 ppm. Así pues, las estaciones 1, 2, 4, 5 y 7 son las que presentaron mayores niveles de concen traciones de Cromo promedio anual.
Tabla No. 5
Cromo en sedimentos
Cromo en sedimentos

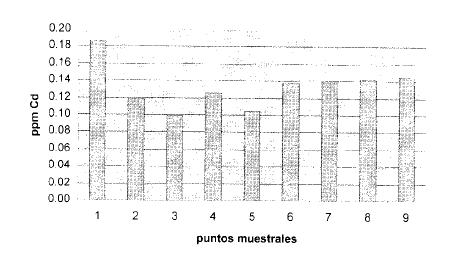
Cadmio
En el primer muestreo se registraron valores de 0.182 ppm en la estación # 1 y 0.171 en la estación # 4. En el resto de las estaciones se registraron valores por debajo del punto de detección del espectrofotómetro utilizado es decir valores menores que 0.001 ppm . Esto nos indica que la presencia de este metal fue insignificante. En el segundo muestreo todas las estaciones registraron valores por debajo del punto de detección. Igual tendencia se registró en casi todos los muestreos a excepción del de Febrero 2003 y el de Septiembre de 2003. En el cuarto muestreo de Febrero, la concentración promedio de las estaciones fue de 0.97 ppm, en tanto que en el muestreo de Septiembre 2003 solo se detecto la presencia de Cromo en la estacion # 1. Los valores promedio anual por estación fueron 0.19 ppm para la estación # 1, 0.12 ppm para la estación #2, 0.1O ppm para la estación #3; 0.13 ppm para la #4; 0.1O ppm para la #5; 0.14ppm para la #6, 0. 14 ppm para la #7; 0.14 ppm para la #8 y 0.15 ppm para la #9.
Dado que los valores en general estuvieron por debajo del punto de detección, no es posible hablar de ninguna tendencia, salvo el sefialamiento de que sólo en los meses de Octubre 2002, Febrero 2003 y Septiembre 2003 se registró algún valor de concentración de Cadmio. En el caso de los meses Octubre y Septiembre el registro sólo ocurrió en la estación #1, en tanto que en Febrero del 2003 se pudieron registrar niveles de Cadmio en todas las estaciones.
Tabla No. 6
Cadmio en sedimentos
CADMIO EN SEDIMENTOS

Arsénico
Este metal no fue encontrado en ninguna de las estaciones en 7 de los 8 muestreos. En todos esos casos los niveles registrados estaban por debajo del límite de detección del equipo de Absorción Atómica. Sólo en el muestreo correspondiente a Marzo del 2003 fueron encontrados niveles de concentraciones que oscilaron entre 1 .7 ppm y 9.5 174 ppm El valor mínimo correspondió a la estación #9 y el máximo a la estación #7.
Tabla No. 7
Arsénico en sedimentos
ARSENICO EN SEDIMENTO

Zinc
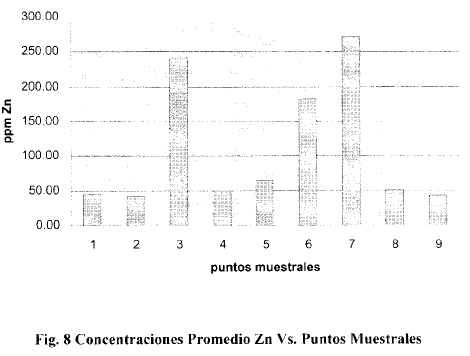
En el primer muestreo los valores de este metal en todas las estaciones estuvieron por debajo del límite de detección del equipo. Sin embargo a partir del segundo muestreo se de terminaron valores significativos. En este segundo muestreo los niveles de Zinc oscilaron entre 40.75 ppm y 226,42 ppm con un promedio para las estaciones de 84.80 ppm. El promedio de las estaciones en el tercer muestreo (Diciembre 2002) estuvo situado en 115.78 ppm, en tanto que en Febrero 2003 descendió a 83.28 ppm, manteniéndose dentro de los mismos límites en Marzo con un valor de 88.65 ppm. En Mayo se produce un ligero ascenso en el valor promedio de las estaciones, descendiendo en Julio a 76.39 ppm, elevándose luego considerablemente en el mes de Septiembre con un valor promedio de 366.14 ppm. Conviene destacar que en el muestreo de Septiembre se registraron en las estaciones 3, 6 y 7 valores de ppm, 256.43 ppm y 1,239.70 ppm respectivamente, los cuales son considerablemente altos con respecto a la media de las otras estaciones, en el mismo muestreo, que estuvo por debajo de 45 ppm. Es evidente aquí que a excepción del muestreo de Diciembre, los valores promedio de las estaciones fueron similares oscilando dichos promedios entre 76.39 y 90.71 ppm. El promedio anual por cada estación fue el siguiente: 44.61 ppm para la estación # l ; 41 .27 ppm para la estación #2; 240.77 ppm para la estación #3; 49.66 ppm para la estación #4; 64.02 ppm para l a #5; 183.27 para la #6; 271 .91 ppm para la #7; 50.33 ppm para la #8 y 43.80 para la #9.
Tabla No. 8
Zinc en sedimentos

ZINC EN SEDIMENTOS

Metales en agua
Hierro
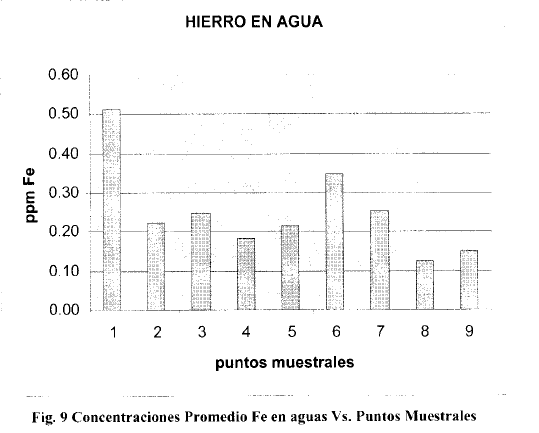
Respecto a los puntos muestrales, la máxima concentración de Fe fue detectada en la Estación #6 durante el primer muestreo, con un valor de 0.7367 ppm. En el tercer muestreo el va lor máximo se reportó en la Estación #1 con un valor de 3.7034 ppm. En el muestreo de Marzo el valor máximo se encontró de nuevo en la estación #6 con un valor de 1.3133 ppm. En el muestreo de Julio, la mayor concentración fue encontrada en la Estación #2 con un valor de 1.1531ppm En algunos casos, las concentraciones exceden los límites máximos permitidos para la vida acuática de agua dulce de acuerdo a las normas de Brasil (CONAMA 20/1986) y Canadá ( 1987) que establecen el standard para este metal en aguas de río en 0.3ppm. Sin embargo, los valores registrados se mantienen por debajo de los stándares de República Dominicana (NORDOM 436) y de la Comunidad Económica Europea (CEE 1975/440) que fijan el valor máximo de este metal en 2ppm.
Sólo se detectó la presencia de Hierro en todos los puntos muestrales en el 50% de los muestreos (muestreos 1,3, 7 y 8). Las más altas concentraciones fueron encontradas en Diciembre 2002(muestreo 3) y en Marzo 2003 (muestreo 5) y en Julio 2003(Muestreo 7).
Esencialmente los niveles encontrados en agua fueron relativamente bajos en la mayoría de muestreos. Esto se explica por la tendencia natural de los metales a preci pitar y su escasa solubilidad en agua. En el primer muestreo los valores oscilaron entre 0.0827 ppm y 0.7367 ppm para un valor promedio de estaciones de 0.30 ppm. En el segundo m uestreo, todas las estaciones registraron valores por debajo del límite de detección del equipo que es de 0.001ppm. En el tercer muestreo correspondiente a Diciembre, los valores oscilaron entre 0.0232 ppm y 3.7034, con un valor promedio de estaciones de 0.53 ppm. En Febrero los valores registrados también estuvieron por debajo del límite de detección para todas las estaciones. En Marzo se registraron valores pequeños oscilantes entre el límite de detección y 1.31 ppm, para un promedio de estaciones de 0.59 ppm. El muestreo de Mayo también reflejó valores por debajo del límite de detección. En el muestreo de Julio los valores oscilaron entre 0.19 1ppm y 1.1531 ppm para un promedio de 0.37 ppm, en tanto que en el muestreo de Septiembre ese valor promedio de estaciones estuvo situado en 0.27 ppm.
Tabla No. 9
Hierro en aguas
HIERRO EN AGUA

Cobre
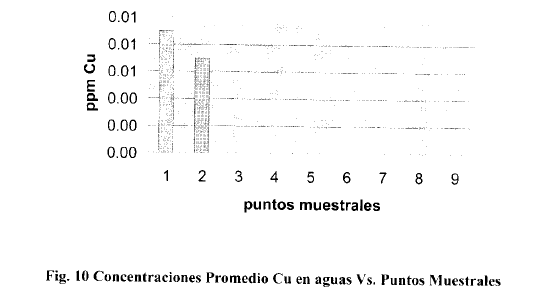
En la mayoría de muestreos los valores detectados para todas las estaciones estuvieron por debajo de 0.001 ppm, límite de detección del equipo. Las excepciones se presentaron en el tercer muestreo de Diciembre del 2002 en el cual en las estaciones 1 y 2 se registraron valores de 0.0135 ppm y 0.0301 ppm respectivamente. De igual manera en el muestreo de Marzo se registró un único valor de 0.0179 ppm en la estación 1. Finalmente en el muestreo de Septiembre del 2003, las estaciones 1 y 2 registraron valores de 0.0389 ppm y 0.0274 ppm. Se puede concluir que la presencia de Cobre en las aguas fue irrelevante en todos los muestreos.
En todos los casos en que se registraron valores por encima del punto de detección del equipo, éstos superan los máximos permitidos para la vida acuática de agua dulce en las normas de Canadá (0.002 a 0.004 ppm) y se mantienen por debajo de los máximos de NORDOM 436 (2 ppm)
Tabla No. 10
Cobre en aguas
COBRE EN AGUAS

Otros metales en aguas
En la totalidad de los muestreos, ninguno de los otros metales estudiados fueron detectados en las aguas de las diferentes estaciones.
Valores estándares de metales pesados en sedimentos
Se utilizaron los valores estándares establecidos por la Canadian Environmental Quality Guidelines(ISQG -Interim Se diment Quality Guideline). A continuación se presenta una tabla con dichos valores.
El 97.22% de las muestras de Cobre en sedimentos se encuentran en por encima del valor standard que es 35.7 ppm, por lo cual puede considerarse el Río Haina como altamente contaminado por Cobre. En el caso del Plomo en sedimientos, el 25% de las muestras registró niveles por encima del valor stándard de 35 ppm. El 100% de las muestras de Cromo en sedimentos estuvo por encima del standard que es 37.3 ppm, lo que significa altamente contaminadas. 12.5% de las muestras de Cadmio en sedimentos registraron valores por encima del standard que es 0.6 ppm. Sólo el 4.16% de l as muestras de Arsénico registró valores por encima del standard que es 5.9 ppm. El 13.88% de las muestras registró valores de Zinc por encima del stándard que es 123 ppm.
Valores standares de metales pesados en aguas

Sólo una (1) de 72 muestras de Hierro en aguas registró valores por encima del valor standard de 2.0 ppm, en tanto que el 100% de las muestras de Cobre en aguas registró valores por debajo del standard máximo de 2.0 ppm.
Conclusiones
1. Existen altos niveles de concentraciones de metales pesados en los sedimentos del Río Haina. Estos valores están en la mayoría de los casos por encima de los stándares internacionales, lo cual implica alta contaminación de dicho río por metales pesados.
2. Se encontraron bajos niveles de metales pesados en las aguas del Río Haina, valores que se encuentran por debajo de los stándares nacionales. Los bajos niveles de metales pesados en las aguas se explican por la baja so lubilidad de estos metales en ese líquido y la tendencia natural de ellos a precipitar y acumularse en los sedimentos.
3. En el caso de los sedimentos existe una variación pronunciada con las estaciones del año. Los más altos niveles se registraron en los meses de verano e invierno.
4. Se aprecian diferencias considerables entre los valores de las diferentes puntos muestrales en un mismo muestreo.
5. Existe un riesgo para la pesca dado que los peces se alimentan entre otras fuentes de los sedimentos. Los metales pesados pueden bioacumularse en los peces que se alimentan de los sedimentos y traer implicaciones serias para la salud de las personas que consuman dichos peces.
6. En las aguas sólo fueron detectados los metales Hierro y Cobre.
7. El Arsénico en sedimentos sólo fue detectado en un solo muestreo, el correspondiente al mes de marzo. Sólo el 4.16% de las muestras de Arsénico registró valores por encima del standard que es 5.9 ppm.
8. El Cadmio en sedimentos sólo fue detectado en tres de los ocho muestreos en uno de los cuales fue detectado en todas l as estaciones, en los otros muestreos se le detectó sólo en algunas puntos muestrales. El 12.5% de las muestras de Cadmio en sedimentos registró valores por encima del standard que es 0.6 ppm.
9. El 97.22% de las muestras de Cobre en sedimentos se encuentra por encima del valor standard que es 35.7 ppm, por lo cual puede considerarse el Río Haina como altamente contaminado por Cobre.
10. El 25% de las muestras registró niveles de Plomo por encima del valor stándard de 35 ppm.
11 . El 100% de las muestras de Cromo en sedimentos estuvo por encima del standard que es 37.3 ppm, lo que significa que el Río Haina está altamente contaminado por ese metal.
12. El 13.88% de las muestras registró valores de Zinc por encima del stándard que es 123 ppm.
Agradecimientos
Los autores agradecen al Instituto Tecnológico de Santo Domi ngo (Intec) el financiamiento de la investigación. De igual manera agradecen al Dr. rogelio Cid, la Licenciada Francia Gómez y a las Srtas. Rita iris Pérez y Beatriz Melo por su valiosa colaboración.
Bibliografía
1.Barber, William P.; David C. Stuckey. “Metal bioavailability and trivalent chromium removal” Journal of Environmental Engineering, v. 126 i5, July 2000, p649(8)
2.Bello Bugallo, P.M.; J. A. Souto González; J. J. Long Casares; T. Lucas Domínguez “Análisis preliminar de la movi1ización/ deposición de metales pesados en el sistema río Etime-embalse: Aplicación al manganeso”. Afinidad: revista de química teórica y aplicada. SI. (4h6): 115.22, mar.abr., 2000
3.Borg, L. G. ; Jorgen Ek ; Elizabeth Froberg: Karin Holm; AnnMarie Johansson; Pia, Karrhage; Goran Rosen; Maria, Soderstrom “The turnover of nietals in a eutrophic and an oligotrophic lake in Sweden” Ambio, V. 29, i4-5, August 2000, p 217 (13)
4.Brian P. B. “Removal of heavy metals from water: an environmentally significant absorption spectrometry experiment” Journal of Chemical Education V76 i12, Dec, 1999, p1678(2)
5.Campos C. Néstor Hernando. “Concentraciones de metales traza en Ariopsis bonillai (Pisces Siluriformes) de Santa Marta, Caribe colombiano” Revista de Biología Tropical, 40 (2): 179-83, ago., 1992
6.Cervantes, Carlos; Jaime Chávez; Sergio Vaca. “Mecanismos de resistencia bacteriana a metales pesados “Revista Latinoamericana de Microbiología, 33. (1): 61-70, ene.-mar..1991
7.Dey, S.; S. K. Dwivedi “Toxic metals in Hens’Eggs in India: A preliminary Report”. Archives of Environmental Health V. SS i5 Sept 2000, p365
8.Kady El; G. Al Ahmadi; T. A. A. Odozi “Effect of heavy metalion concentration and pH values on the sorption behaviour of prepared exchangers” Afinidad, 50. (447): 296-3M, sept. -oct,. 1993
9.Lazaro, M. J.; R. Moliner, I. Duelves; C. Nerin. “Valuable products from mineral waste oils containing heavy metals”. Environmental Sciencie & Technology v. 35 i15, August 1, 2000 p3205 6)
10.Mag, Coll. “Death metal”. Environment V41 i9, Nov 1999, p6
11.Mendoza de Cid, Leticia; Bélgica N3ut M. “Determinación de elementos químicos en las aguas del río Ozama mediante la técnica de fluorescencia ‹te rayos-X por reflexión total (TRXRF) Revista Ciencia y Sociedad Vol. xviii, No. 1 Enero-Marzo (1993) Pág.49.
12.Mondaca, María Angélica; Mireya, Abarzua: Karina, Paredes; Teresa Maugeri; Miguel, Martínez “Transferencia de resistencia a metales pesados en bacterias aisladas del río BíoBío viii Región, Chile. Revista Latinoamericana de Microbiología 35. (1): 39-43, ene-mar.,1993
13.Obiols Salvat, José; R., Devesa; L. Peirot; J. Salayet “Especiación de metales pesados. i.. Conceptos y técnicas”Afinidad, Vol. 44, (408): 93-6, mar-abr., 1987
14.Obiols Salvat, José; R., Devesa; Salayet, J.”Especiación de metales pesados. ii. en agua de mar” Afinidad Vol. 44 (409): 191-4, mayo-jun., 1987
15.Romana Ruiz, Manuel “Contaminación en sedimentos marinos” Revista de Obras Públicas, 141. (3329): 21-30, feb, 1994.
16.Ruiz, F.., F., Romero; A. Fcheandía “Composición, distribución por tamaños, contenido en metales pesados y características de sedimentos de la cuenca del río Bidasoa “Afinidad, 49. (442): 361371, nov.-dic., 1992.
