Ciencia y Salud, Vol. 10, No. 1, enero-abril, 2026 • ISSN (impreso): 2613-8816 • ISSN (en línea): 2613-8824
TUMOR SÓLIDO PSEUDOPAPILAR DE PÁNCREAS: ABORDAJE QUIRÚRGICO DE UNA NEOPLASIA RARA. REPORTE DE CASO
Solid pseudopapillary tumor of the pancreas: surgical approach to a rare neoplasm. Case report
DOI: https://doi.org/10.22206/cisa.2026.v10i1.3512
Recibido: 08/04/2025 • Aceptado: 11/06/2025
Cómo citar: Castillo de los Santos, C., Martínez Bisonó, G., Morillo Marte, G. (2026). Tumor sólido pseudopapilar de páncreas: abordaje quirúrgico de una neoplasia rara. Reporte de caso. Ciencia y Salud, 10(1), 65-75. https://doi.org/10.22206/cisa.2026.v10i1.3512
Resumen
Problema: El tumor sólido pseudopapilar de páncreas, también conocido como tumor de Frantz-Gruber, es una neoplasia pancreática extremadamente rara que representa menos del 1 % de los tumores pancreáticos. Predomina en mujeres jóvenes y suele diagnosticarse incidentalmente mediante estudios de imagen. Caso clínico: Se presenta el caso de una paciente de 24 años con síntomas de dispepsia, náuseas y obstrucción de la salida gástrica. Los estudios de imagen evidenciaron una lesión solidoquística de 69x59 mm en la cabeza del páncreas con signos de infiltración en la curvatura menor del estómago y al peritoneo adyacente con múltiples adenopatías mesentéricas. Hallazgos: Se realizó una pancreatoduodenectomía con reconstrucción en Y de Roux. El estudio histopatológico confirmó el diagnóstico de tumor sólido pseudopapilar con positividad para β-catenina nuclear y receptores de progesterona. La pieza resecada no evidenció infiltración a otros órganos y los márgenes quirúrgicos fueron negativos (R0). La paciente presentó una evolución posoperatoria favorable, siendo dada de alta sin complicaciones mayores y con seguimiento ambulatorio sin evidencia de recurrencia hasta la fecha. Conclusión: La cirugía sigue siendo el tratamiento de elección, con una tasa de sobrevida a 5 años superior al 90 %, incluso en presencia de metástasis. Este caso subraya la importancia del diagnóstico oportuno y el abordaje quirúrgico completo para optimizar el desenlace clínico de estos pacientes.
Palabras clave: Tumor sólido, pseudopapilar, tumor de Frantz-gruber, neoplasia pancreática, pancreatoduodenectomía, baja malignidad.
Abstract
Problem: Solid pseudopapillary tumor of the pancreas, also known as Frantz-Gruber tumor, is an extremely rare pancreatic neoplasm that accounts for less than 1 % of pancreatic tumors. It predominates in young women and is usually diagnosed incidentally through imaging studies. Clinical case: We present the case of a 24-year-old patient with symptoms of dyspepsia, nausea, and gastric outlet obstruction. Imaging studies showed a 69x59 mm solidocystic lesion in the head of the pancreas with signs of infiltration into the lesser curvature of the stomach and the adjacent peritoneum with multiple mesenteric lymphadenopathies. Findings: A pancreaticoduodenectomy with Roux-en-Y reconstruction was performed. Histopathological examination confirmed the diagnosis of solid pseudopapillary tumor with positivity for nuclear β-catenin and progesterone receptors. The resected specimen did not show evidence of infiltration into other organs, and the surgical margins were negative (R0). The patient had a favorable postoperative course and was discharged without major complications. She has been followed up as an outpatient without evidence of recurrence to date. Conclusion: Surgery remains the treatment of choice, with a 5-year survival rate of over 90 %, despite metastatic disease. This case underscores the importance of timely diagnosis and a comprehensive surgical approach to optimize the clinical outcome of these patients.
Keywords: Solid tumor, pseudopapillary, Frantz-gruber tumor, pancreatic neoplasia, pancreaticoduodenectomy, low malignancy.
Introducción
El tumor sólido pseudopapilar de páncreas, reconocido por la Organización Mundial de la Salud (OMS) y conocido históricamente como tumor de Frantz o de Frantz-Gruber, es una neoplasia exocrina pancreática rara que representa entre el 0.2 % y el 2.7 % de todas las neoplasias pancreáticas1. Es importante señalar que, en adultos, aunque pueden aparecer en cualquier localización, los TSP ocurren más frecuentemente en el cuerpo o la cola pancreática2. Descrito por primera vez en 1959, se presenta con mayor frecuencia en mujeres jóvenes, con mayor incidencia entre la segunda y cuarta décadas de vida3, 4. Histológicamente, se caracteriza por una mezcla de áreas sólidas con zonas pseudoquísticas, estructuras pseudopapilares y regiones hemorrágicas, así como una red microvascular que forma pseudorrosetas y células eosinófilas o espumosas4.
Clínicamente, los síntomas son a menudo inespecíficos y se deben al efecto de masa del tumor, que se manifiesta típicamente como dolor abdominal vago y sensación de plenitud1. En muchos casos, el diagnóstico se realiza incidentalmente a través de estudios de imagen como la tomografía computarizada (TAC) y la resonancia magnética, aunque en ocasiones puede ser confundido con otros tumores quísticos del páncreas, como los pseudoquistes3. Es relevante mencionar que los marcadores tumorales séricos, como el CA19-9, suelen ser normales en pacientes con TSP, lo que ayuda a su diferenciación de otras neoplasias pancreáticas4. La resección quirúrgica completa del tumor es el tratamiento estándar, ya que esta intervención ofrece una excelente tasa de supervivencia a largo plazo, con una sobrevida a 5 años superior al 90 %3, 4.
Objetivo
Describir el caso clínico de una paciente con un tumor sólido pseudopapilar de páncreas, detallando los hallazgos diagnósticos y el abordaje quirúrgico.
Presentación de caso
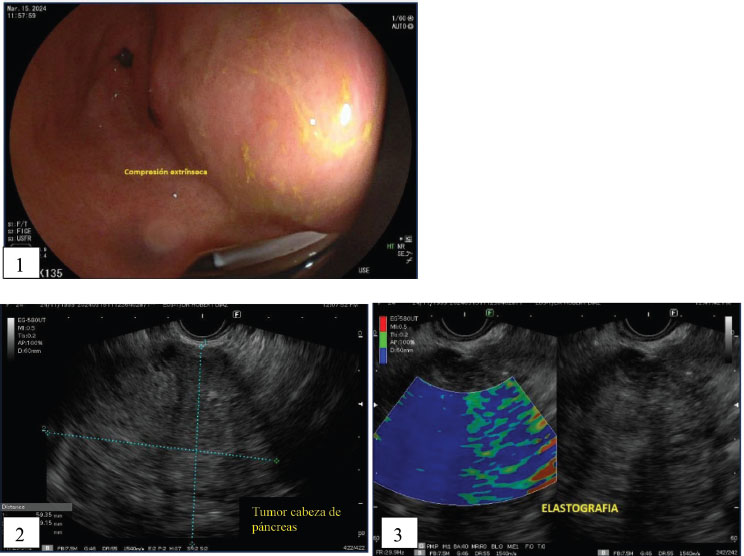
Se trata de una paciente femenina de 24 años, sin antecedentes mórbidos conocidos, con historia de dispepsia, náuseas y signos de obstrucción de la salida gástrica. Es referida al servicio de cirugía general por el departamento de gastroenterología debido a la presencia de un tumor de gran tamaño, de 69x59 mm de diámetro, en la cabeza del páncreas, que desplazaba el estómago y el duodeno, identificado mediante ultrasonografía endoscópica (Figura 1-3), con varios meses de evolución. Los hallazgos imagenológicos evidenciaron una lesión solidoquística irregular e hipoecogénica, en el cuerpo y parte de la cabeza del páncreas. Se observó infiltración en la curvatura menor del estómago y el peritoneo adyacente, acompañada de múltiples adenopatías mesentéricas. Su examen físico presenta un abdomen semi-globoso, dolor en nasogástrico a la palpación, peristalsis adecuada, depresible, no masas palpables, no visceromegalia valorable. Dada la presentación clínica y radiológica, la decisión sobre el manejo diagnóstico invasivo no fue tomada en consideración, por lo que, en este caso, no se realizó una biopsia de la lesión antes de la intervención quirúrgica. Los resultados de laboratorio preoperatorios fueron normales, incluyendo hemograma, función hepática y marcadores tumorales como CA19-9, que se encontró dentro de los rangos de referencia.
Figuras 1-3. En figura 1 se aprecia la comprensión extrínseca del tumor en la cabeza del páncreas. En figuras 2 y 3 se evidencia la lesión hipoecogénica, irregular, de 69 x 59 mm de diámetro, con elastografía predominante azul sugestivo de tumor de consistencia dura. (Ultrasonografía endoscópica)
Descripción del procedimiento quirúrgico
La paciente fue programada para laparotomía exploratoria y pancreatoduodenectomía, con la adición de gastrectomía parcial, colecistectomía, anastomosis pancreato-yeyunal, anastomosis bilio-entérica, anastomosis gastroyeyunal y anastomosis yeyunoyeyunal, y lavado peritoneal terapéutico. Se administró profilaxis antibiótica con cefazolina 1 g IV y metronidazol 500 mg IV. Bajo anestesia general inhalatoria, el procedimiento se inició vía laparoscópica para evaluar la resecabilidad del tumor. Tras la insuflación de la cavidad abdominal con CO2 y la colocación de puertos laparoscópicos, se confirmó una voluminosa lesión pancreática con adherencias.
Dada la magnitud y características de la lesión, se decidió convertir a laparotomía, realizando una incisión tipo Chevron. Tras transgredir los planos anatómicos y acceder a la cavidad abdominal, se confirmaron los hallazgos preoperatorios. Se procedió de inmediato a liberación de bridas y adherencia mediante bisturí harmónico. Se realizó la maniobra de Cattell-Braasch exponiendo complejo pancreático duodenal (Figura 4). Se efectuó la resección del estómago y duodeno, debido a la sospecha preoperatoria de infiltración, así como la disección pancreática distal y proximal de la cabeza. Se disecaron la vena mesentérica superior y la vena porta. Se disecó el aspecto posterior de la cabeza del páncreas, se realizó la colecistectomía y se seccionó el colédoco. La vesícula biliar fue liberada de su lecho hepático con electrocauterio, y se realizó una omentectomía parcial mediante ligadura con seda.
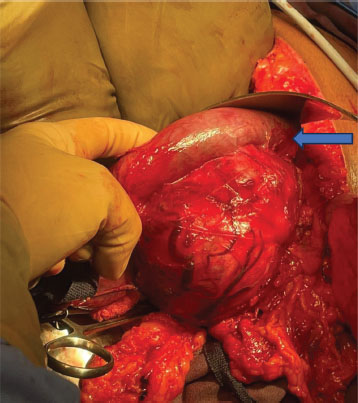
Figura 4. Maniobra de Cattell-Braasch con exposición del complejo pancreático duodenal (flecha azul) tras la movilización medial del colon derecho y la raíz del mesenterio
Durante la exploración intraoperatoria, se identificó una gran masa encapsulada en la cabeza del páncreas, de consistencia firme y bien delimitada, confirmando la extensión y las características neoplásicas observadas en los estudios preoperatorios. Macroscópicamente, no se evidenció invasión franca a estructuras vitales adyacentes más allá de la porción gástrica resecada preventivamente, ni adenopatías sospechosas adicionales fuera de las ya identificadas en el mesenterio. Se extrajo la pieza de patología con un tamaño de 9 x 9 cm (Figura 5). La técnica quirúrgica empleada fue una pancreatoduodenectomía clásica (no preservadora de píloro), dada la extensión tumoral y la necesidad de asegurar márgenes oncológicos adecuados.
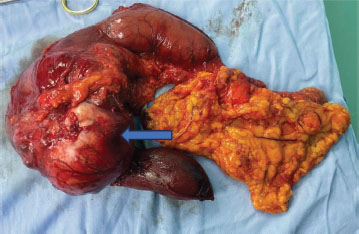
Figura 5. Exposición de la pieza quirúrgica tras su resección. Se aprecia la gran masa encapsulada en la cabeza del páncreas (señalada por la flecha azul), junto con las estructuras comprometidas, incluyendo complejo pancreático duodenal, segmento distal del estómago y tejido adiposo mesentérico
Posteriormente, se procedió a la reconstrucción en Y de Roux, realizando una anastomosis pancreato-yeyunal término-lateral. Se efectuó una anastomosis colédoco-yeyuno término-lateral. Se seccionó el asa yeyunal con sutura mecánica lineal. Se realizó una anastomosis laterolateral de estómago a yeyuno con sutura mecánica lineal. Se confeccionó una Y de Roux realizando una anastomosis de yeyuno a yeyuno con sutura mecánica lineal.
Se realizó un lavado de la cavidad abdominal con solución salina estéril. Se introdujo una sonda naso-yeyunal hasta unos 20 cm después de la anastomosis distal. Se colocó un dren de Blake con su respectivo reservorio, fijándose a la piel. Luego del conteo completo de gasas (20) y compresas (25), se procedió al cierre por planos anatómicos: peritoneo y fascias profundas 0, fascia superficial, cierre umbilical, tejido celular subcutáneo, y piel.
La paciente toleró el procedimiento sin eventualidades. La pérdida sanguínea aproximada fue de 400 ml. El tiempo operatorio estimado fue de 8 horas. La herida quirúrgica fue cubierta con Fusibact y Medipore. El informe anatomopatológico posterior confirmó la resección completa (R0) de la lesión, con márgenes quirúrgicos libres de tumor. La lesión se encontraba a una distancia segura de los márgenes de resección, lo cual es crucial para el pronóstico de este tipo de tumor.
Reporte de patología
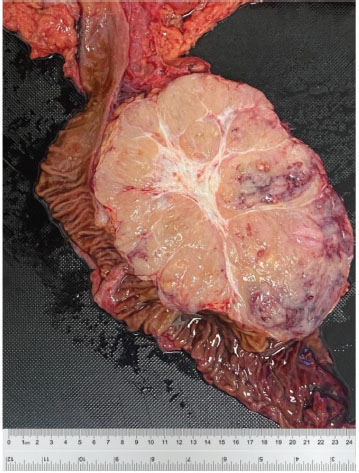
Descripción Macroscópica: Pieza que corresponde a procedimiento de Whipple (Pancreato-duodenectomía), con segmento distal del estómago, duodeno, cabeza de páncreas, vesícula biliar y omento (Figura 6). El segmento de estómago mide 12 x 5 cm, el duodeno con 26 cm de longitud por 4 cm de calibre externo y el páncreas de 10 x 9 cm. A la apertura se observa un tumor circunferencial que ocupa casi todo el páncreas y mide 9 x 9 cm. Este tumor es lobulado, amarillento pardo con área central cicatricial, y se encuentra a 2 cm del margen distal pancreático. Adherido a la curvatura menor del estómago se recibe omento que mide 24 x 18 cm. Se aíslan 3 ganglios peri-pancreáticos.
Figura 6. Pieza de pancreatoduodenectomía (procedimiento de Whipple), incluyendo segmento distal del estómago, duodeno, cabeza de páncreas, y omento
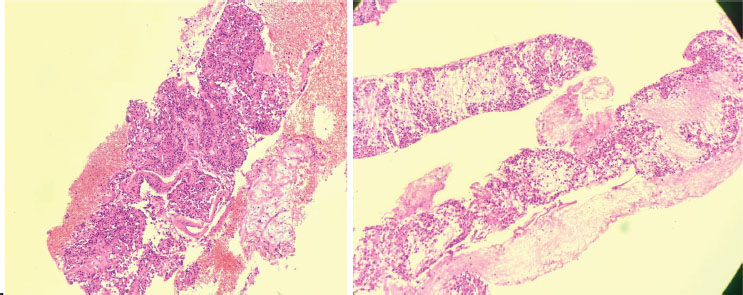
Descripción Microscópica: Se observa páncreas con arquitectura alterada por presencia de neoplasia epitelial maligna formada por células que tienen en áreas vacuolas que desplazan el núcleo, algunos con contornos irregulares. Estos nidos tumorales están separados por septos fibrosos en áreas con agujas de colesterol y macrófagos espumosos (Figura 7-8). Es crucial destacar que no se observó infiltración a otros órganos en la pieza resecada, incluyendo el segmento gástrico y el omento que se resecó debido a la sospecha preoperatoria
Figura 7-8. Tinción con hematoxilina-eosina (H&E). Las imágenes muestran tejido tumoral con un patrón pseudopapilar característico. Se observan grupos de células epiteliales dispuestas alrededor de ejes fibrovasculares, separados por finos septos de tejido conectivo. Las células presentan núcleos redondos u ovalados, algunos con contornos irregulares, y cromatina fina. También se aprecian capilares de paredes delgadas distribuidos entre los nidos celulares
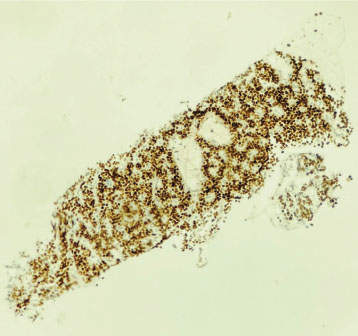
Citología e Inmunohistoquímica: Las imágenes citológicas en base líquida SurePath mostraron agrupaciones tridimensionales de células epiteliales con núcleos aumentados de tamaño y prominentes, compatibles con una lesión epitelial pseudopapilar (Figuras 9-10). La inmunohistoquímica fue determinante: se encontró positividad nuclear para β-catenina (Figura 11) y positividad nuclear para receptores de progesterona (Figura 12), hallazgos consistentes y prácticamente patognomónicos del tumor pseudopapilar de páncreas5. Otros marcadores típicamente positivos en el tumor pseudopapilar de páncreas, como la vimentina y CD99, no fueron evaluados en este caso.
Figura 9-10. Citología en base líquida SurePath. Las imágenes citológicas muestran agrupaciones tridimensionales de células epiteliales con núcleos aumentados de tamaño y prominentes. Se observan características celulares compatibles con una lesión epitelial de tipo pseudopapilar, con núcleos redondeados y nucléolos visibles. Algunas células presentan citoplasma denso y disposición en grupos cohesivos. La tinción resalta la morfología nuclear y citoplasmática, útil para el diagnóstico citológico
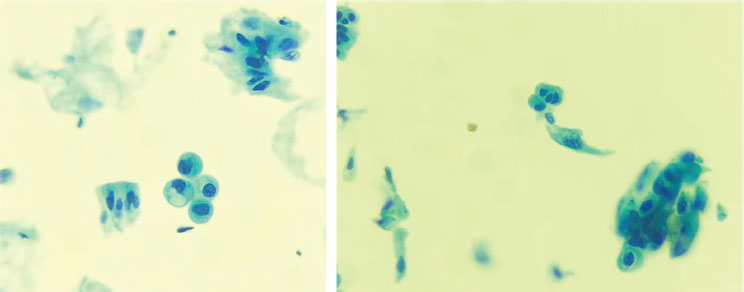
Figura 11. Inmunohistoquímica para beta-catenina. La imagen muestra una tinción inmunohistoquímica positiva para beta-catenina. Se observa una coloración marrón predominante en las membranas celulares y parcialmente en los núcleos, indicando la localización de esta proteína. Las células están organizadas en grupos cohesivos, y la tinción resalta tanto la morfología nuclear como la citoplasmática, lo cual es útil para el diagnóstico citológico de procesos neoplásicos
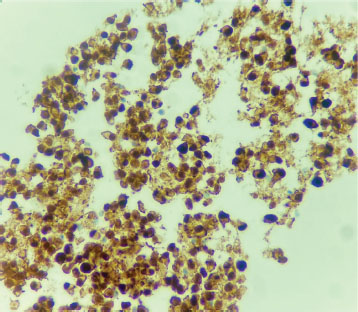
Figura 12. Inmunotinción positiva nuclear para receptores de progesterona en células neoplásicas. En esta imagen se observa una tinción inmunohistoquímica con positividad nuclear, lo que indica la presencia de receptores de progesterona en las células tumorales. La coloración marrón se localiza específicamente en los núcleos de las células, lo cual es característico de una respuesta positiva en este tipo de análisis. Esta información es importante para la caracterización hormonal de ciertos tipos de neoplasias, como las del aparato reproductor femenino
Discusión
El tumor sólido pseudopapilar de páncreas, o tumor de Frantz-Gruber, es una neoplasia rara que representa entre el 0.2 % y el 2.7 % de los tumores exocrinos pancreáticos, con una clara predilección por mujeres jóvenes entre la segunda y cuarta décadas de vida4. A diferencia de la mayoría de las neoplasias pancreáticas, este tumor se distingue por su crecimiento lento y su bajo potencial maligno. Aunque generalmente presenta un pronóstico favorable, cabe señalar que existe un riesgo del 10 % de que desarrolle características malignas6. Su baja incidencia y la inespecificidad de sus síntomas dificultan su diagnóstico temprano, lo que hace que muchas veces sea un hallazgo incidental en estudios de imagen realizados por otros motivos4, 5. Desde el punto de vista clínico, el tumor sólido pseudopapilar de páncreas suele presentarse con síntomas inespecíficos como dolor abdominal, náuseas, vómitos y sensación de plenitud5. La sintomatología suele deberse al efecto de masa que genera el tumor cuando alcanza un tamaño significativo5. En algunos casos, puede ocasionar síntomas más severos, como obstrucción de la salida gástrica, tal como se observó en la paciente de este reporte.
El tumor sólido pseudopapilar de páncreas afecta el tejido exocrino pancreático, que está compuesto por células acinares encargadas de producir enzimas digestivas. Estas células tienen una forma piramidal y contienen gránulos rodeados por una membrana, que alberga sustancias como tripsinógeno, quimotripsinógeno, procarboxipeptidasa, proelastasa, calicreinógeno y profosfolipasas A y B6. Los tumores sólidos pseudopapilares suelen presentar una combinación de elementos, incluyendo áreas hemorrágicas y calcificaciones, así como una cápsula fibrosa7. A nivel celular, es común observar vacuolas citoplasmáticas, núcleos granulares y glóbulos hialinos, características que ayudan a su diagnóstico8, 9. Además, se encuentran células monomórficas de tamaño pequeño a mediano, dispuestas sobre un fondo limpio o hemorrágico, y estructuras papilares10. El diagnóstico definitivo se logra mediante estudios inmunohistoquímicos que detectan principalmente la mutación de la proteína β-catenina10.
El diagnóstico de tumor sólido pseudopapilar de páncreas se apoya principalmente en estudios de imagen11. La ecografía abdominal puede revelar una masa heterogénea con componentes sólidos y quísticos11. Sin embargo, la tomografía computarizada (TAC) y la resonancia magnética (RM) ofrecen una caracterización más detallada de la lesión, evidenciando una neoplasia de bordes bien definidos, de consistencia mixta y vascularidad periférica11. Estas características ayudan a diferenciar el tumor sólido pseudopapilar de páncreas de otros tumores pancreáticos más agresivos11.
Desde el punto de vista histopatológico, el tumor sólido pseudopapilar de páncreas exhibe una combinación de áreas sólidas con regiones pseudopapilares y hemorrágicas, además de una red microvascular que forma pseudorrosetas11. El origen celular de la neoplasia sólida pseudopapilar aún no está completamente claro; sin embargo, se sugiere que estas células provienen de células madre pluripotentes situadas en las crestas genitales, las cuales se integran al páncreas durante el desarrollo embrionario12. Se ha observado que la neoplasia sólida pseudopapilar está asociada con mutaciones en el cromosoma 11q, que alberga genes responsables de la producción de proteínas clave, como la ciclina D1, FLI-1, CD56 y el receptor de progesterona13. Asimismo, se ha observado que el tumor pseudopapilar de páncreas está asociado con mutaciones en el exón 3 del gen de la β-catenina (CTNNB1), lo que activa la vía de señalización de Wnt5, 14. La positividad nuclear uniforme para β-catenina en la inmunohistoquímica es un hallazgo casi universal y altamente específico para el diagnóstico del tumor5, 14. Aunque la expresión del receptor de progesterona en la neoplasia sólida pseudopapilar podría explicar su mayor frecuencia en mujeres debido a su sensibilidad a las hormonas, aún no se ha establecido un vínculo claro entre este receptor y la tumorigénesis14, 15. Además, se han identificado mutaciones en el exón 3 del gen de la β-catenina, lo que activa la vía de señalización de Wnt14, 15. Esta vía se ve amplificada por el gen BCL9, presente en los tumores sólidos pseudopapilares, lo que incrementa la actividad transcripcional y favorece la oncogénesis14, 15.
El tratamiento de elección para el tumor sólido pseudopapilar de páncreas es la resección quirúrgica completa con márgenes negativos, lo que garantiza un excelente pronóstico11. Aunque estos tumores se consideran de bajo potencial maligno, en un pequeño porcentaje de los casos pueden desarrollar metástasis, principalmente en hígado y peritoneo10. Sin embargo, incluso en presencia de enfermedad metastásica, la resección sigue siendo una opción viable con altas tasas de supervivencia10. A diferencia del adenocarcinoma ductal pancreático, que representa el 85 % de los tumores exocrinos del páncreas y conlleva una sobrevida media de aproximadamente seis meses, el tumor sólido pseudopapilar de páncreas tiene un pronóstico significativamente más favorable10. La resección quirúrgica completa se asocia con una tasa de sobrevida a cinco años superior al 90 %, incluso en casos donde existe metástasis hepática16. La tasa de recurrencia después de la resección quirúrgica de un tumor sólido pseudopapilar no metastásico es del 2 %17. Los principales factores que aumentan el riesgo de recurrencia incluyen el ser hombre, la presencia de ganglios linfáticos positivos e invasión linfovascular17. Además, el tamaño del tumor, particularmente cuando supera los 5 cm, y las metástasis sincrónicas también se han asociado con un mayor riesgo de recurrencia17. Este contraste subraya la importancia de un diagnóstico preciso, ya que el manejo quirúrgico oportuno puede cambiar radicalmente el desenlace clínico de los pacientes afectados.
Discrepancia Clinicopatológica: Un punto relevante en este caso es la discrepancia entre los hallazgos imagenológicos preoperatorios y el estudio anatomopatológico definitivo. Mientras que las imágenes sugerían "infiltración al estómago y peritoneo", el reporte patológico final indicó "sin infiltración a otros órganos" y márgenes negativos en la pieza resecada. Esta discordancia es un fenómeno conocido y puede deberse a inflamación reactiva o adherencias benignas que simulan infiltración tumoral en las imágenes, o a una invasión microscópica mínima no evidente macroscópicamente pero que justificó la resección de esa porción gástrica para asegurar márgenes oncológicos. La ausencia de invasión en la patología R0 confirmó que la estrategia quirúrgica radical fue efectiva en lograr una resección completa y curativa, a pesar de la interpretación imagenológica inicial. Esta correlación subraya la importancia de la evaluación multidisciplinaria y la confirmación histopatológica definitiva para el manejo óptimo de los pacientes.
Conclusión
El tumor sólido pseudopapilar de páncreas es una entidad poco frecuente, con características clínicas y radiológicas que pueden dificultar su diagnóstico temprano. Su baja agresividad y excelente pronóstico tras una resección completa lo diferencian de otras neoplasias pancreáticas, destacando la importancia de su identificación oportuna. El presente caso ilustra la relevancia de considerar este tumor dentro del diagnóstico diferencial de masas pancreáticas, especialmente en mujeres jóvenes con síntomas inespecíficos. A partir de la experiencia en este caso, se reafirma que la cirugía continúa siendo el tratamiento de elección, asociada a altas tasas de supervivencia y un bajo riesgo de recurrencia, incluso en situaciones de enfermedad metastásica. Este reporte de caso sugiere que el reconocimiento adecuado de esta patología permite un abordaje oportuno que puede mejorar significativamente el desenlace clínico y la calidad de vida de los pacientes.
Financiamiento
Los autores declaran que no recibieron fondos específicos de agencias de financiación en los sectores público, comercial o sin ánimo de lucro para la realización de esta investigación.
Conflictos de intereses
Lo autores declaran no tener ningún conflicto de intereses.
Consideraciones éticas
Se obtuvo el consentimiento informado por escrito de la paciente para la publicación de su caso e imágenes, garantizando su anonimato.
Referencias bibliográficas
1. Fabio H, López DA, San P, Villanueva PB. TUMOR SÓLIDO PSEUDOPAPILAR DE PÁNCREAS. Reporte de caso. Revista de cirugía [Internet]. 2020 Sep 28 [cited 2025 Mar 6];72(5). Available from: https://www.scielo.cl/scielo.php?script=sci_arttext&pid=S2452-45492020000500460
2. Mao J, Li Z, Ma C, Yang Y, Zhao Y, Feng Y, et al. Clinicopathological Features and Surgical Outcomes of Pancreatic Solid Pseudopapillary Neoplasm: A Retrospective Study of 100 Cases. Front Oncol. 2022;12:902345.
3. Álvarez-Pertuz H, Poblete-Otero F, Arana-Sáenz A, Hernández-Ramírez K, Villegas-Bermúdez D. Tumor de Frantz-Gruber, un tumor sólido pseudopapilar del páncreas poco frecuente. Acta Médica Costarricense [Internet]. 2025 [cited 2025 Mar 6];53(3):151–3. Available from: https://www.scielo.sa.cr/scielo.php?script=sci_arttext&pid=S0001-60022011000300008
4. Mazzarella G, D’Andrea D, D’Angelo F, Valente R, Del Basso C, Giovannini I, et al. Solid pseudopapillary tumor of the pancreas: a systematic review of 1384 patients. Langenbecks Arch Surg. 2024 Feb;409(1):151.
5. Miranda-Castillo F, Auria-Aspiazu D, Plaza-Vélez J, Villacís-Muñoz M, Benites-Ordinola C. Tumor de Frantz-Gruber, un tumor sólido quístico pseudopapilar del páncreas infrecuente. Cirujano General [Internet]. 2020 Jan 1 [cited 2025 Mar 6];42(3):223–7. Available from: https://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S1405-00992020000300223
6. Perea Cosío RA, Norberto Rodríguez A, Menchaca Alanís LM, Sarmiento Huizar V, Mendoza García MÁ, Chapa P, et al. Tumor sólido pseudopapilar de páncreas o “‘tumor de Frantz’”. Presentación de dos casos clínicos. Cirujano General [Internet]. 2021 [cited 2025 Mar 10];43(4):265–70. Available from: https://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S1405-00992021000400265
7. Raúl Méndez-Vivas W, Vázquez-Pelcastre R, Escalante-San A, Román, Del M, Pereyra-Balmes C. Tumor de Frantz-Gruber. Reporte de un caso y revisión de la literatura. Evidencia Médica e Investigación en Salud. 2014 [cited 2025 Mar 10];7:143–6. Available from: https://www.medigraphic.com/pdfs/evidencia/eo-2014/eo143j.pdf
8. Padrón Pardo OL, Salamanca Chaparro WH, González Salebe VM, Gutierrez Arias PC, Ramírez Moreno JS, Lúquez Mindiola AJ. Neoplasia sólida pseudopapilar de páncreas: una serie de cinco casos y revisión de la literatura. Revista colombiana de Gastroenterología [Internet]. 2022 Dec 21 [cited 2025 Apr 8];37(4):466–77. Available from: http://www.scielo.org.co/scielo.php?script=sci_arttext&pid=S0120-99572022000400466
9. Santini D, Poli F, Lega S. Tumores sólido-papilares del páncreas: histopatología. JOP 2006;7(1):131-136.
10. Jhala N, Siegal GP, Jhala D. Large, clear cytoplasmic vacuolation. Cancer [Internet]. 2008 May 16 [cited 2025 Apr 8];114(4):249–54. Available from: https://acsjournals.onlinelibrary.wiley.com/doi/10.1002/cncr.23595
11. Meriden Z, Shi C, Edil BH, Ellison T, Wolfgang CL, Cornish TC, et al. Hyaline Globules in Neuroendocrine and Solid-pseudopapillary Neoplasms of the Pancreas. The American Journal of Surgical Pathology [Internet]. 2011 Jun 15 [cited 2025 Apr 8];35(7):981–8. Available from: https://journals.lww.com/ajsp/abstract/2011/07000/hyaline_globules_in_neuroendocrine_and.5.aspx
12. Rosa SL, Bongiovanni M. Pancreatic Solid Pseudopapillary Neoplasm: Key Pathologic and Genetic Features. Archives of Pathology & Laboratory Medicine [Internet]. 2020 Jan 20 [cited 2025 Apr 8];144(7):829–37. Available from: https://meridian.allenpress.com/aplm/article/144/7/829/427491/Pancreatic-Solid-Pseudopapillary-Neoplasm-Key
13. Francisco I, Soledad M, Eulalia M, Augusto E. Neoplasia sólida pseudopapilar de páncreas “Tumor de Frantz”. Reporte de caso. Revista de la Facultad de Ciencias Médicas de la Universidad de Cuenca [Internet]. 2021 Oct 29 [cited 2025 Mar 10];39(2). Available from: https://publicaciones.ucuenca.edu.ec/ojs/index.php/medicina/article/view/3039
14. Tiemann K, Heitling U, Kosmahl M, Klöppel G. Solid pseudopapillary neoplasms of the pancreas show an interruption of the Wnt-signaling pathway and express gene products of 11q. Modern Pathology [Internet]. 2007 Sep [cited 2025 Apr 8];20(9):955–60. Available from: https://www.modernpathology.org/article/S0893-3952(22)03269-0/fulltext
15. Tanaka Y, Kato K, Notohara K, Hojo H, Ijiri R, Miyake T, et al. Frequent β-Catenin Mutation and Cytoplasmic/Nuclear Accumulation in Pancreatic Solid-Pseudopapillary Neoplasm. Cancer Research [Internet]. 2001 Dec [cited 2025 Apr 8];61(23):8401–4. Available from: https://aacrjournals.org/cancerres/article/61/23/8401/508292/Frequent-Catenin-Mutation-and-Cytoplasmic-Nuclear
16. Ruesca C, Lorenzo R, García A, Vásquez A, Fernández M. Carcinoma pseudopapilar sólido del páncreas. Revista Médica Electrónica [Internet]. 2021 [cited 2025 Mar 10];43(2):3270–8. Available from: http://scielo.sld.cu/scielo.php?script=sci_arttext&pid=S1684-18242021000203270
17. Natesh Yepuri, Naous R, Meier AH, Cooney RN, Dilip Kittur, Are C, et al. A systematic review and meta-analysis of predictors of recurrence in patients with Solid Pseudopapillary Tumors of the Pancreas. HPB [Internet]. 2019 Jul 23 [cited 2025 Apr 8];22(1):12–9. Available from: https://www.hpbonline.org/article/S1365-182X(19)30592-1/fulltext
_______________________________
1 Clínica Corominas, Santiago de los Caballeros, República Dominicana. ORCID: https://orcid.org/0009-0002-8107-1291, email: castillodelossantos@gmail.com
2 Pontificia Universidad Católica Madre y Maestra, Santiago de los Caballeros, República Dominicana. ORCID: https://orcid.org/0009-0008-3973-3144, email: gabriela.martinez090820@gmail.com
3 Clínica Corominas, Santiago de los Caballeros, República Dominicana. ORCID: https://orcid.org/0009-0003-0201-1408, email: gladys_morillo@hotmail.com
